Forscher aus Heidelberg und Grenoble beschreiben eine Teilstruktur des "zellulären Briefträgers" SRP
Dr. Klemens Wild und Prof. Dr. Irmgard Sinning (Biochemie-Zentrum der Universität Heidelberg) und Dr. Stephen Cusack (EMBL Grenoble) berichten in der heutigen Ausgabe der Zeitschrift Science über die hochaufgelöste Kristallstruktur eines Protein-RNA-Komplexes des humanen "signal recognition particle (SRP)"
Die Autoren Dr. Klemens Wild und Prof. Dr. Irmgard Sinning vom Biochemie-Zentrum der Ruprecht-Karls-Universität Heidelberg (BZH) und Dr. Stephen Cusack, Leiter der Zweigstelle des Europäischen Molekularbiologischen Labors (EMBL) in Grenoble, berichten in der aktuellen Ausgabe der Zeitschrift Science vom 19. Oktober 2001 über die hochaufgelöste Kristallstruktur eines Protein-RNA-Komplexes des humanen "signal recognition particle (SRP)". (Crystal structure of an early protein-RNA assembly complex of the signal recognition particle)
Leben beruht auf der Abgrenzung von, und der Kommunikation von Zellen mit ihrer Umgebung. Ein wichtiger Prozess hierbei ist die Zielsteuerung von Proteinen in und durch Zellmembranen. Für den Transport enthalten diese Proteine eine amino-terminale Signalsequenz, die wie eine Postleitzahl ihren Zielort bestimmt. Der in allen Domänen des Lebens vorhandene zelluläre Briefträger ist das "signal recognition particle" (SRP), in Säugetieren ein zytosolischer Komplex bestehend aus einer Ribonukleinsäure (SRP-RNA) und sechs Proteinen.
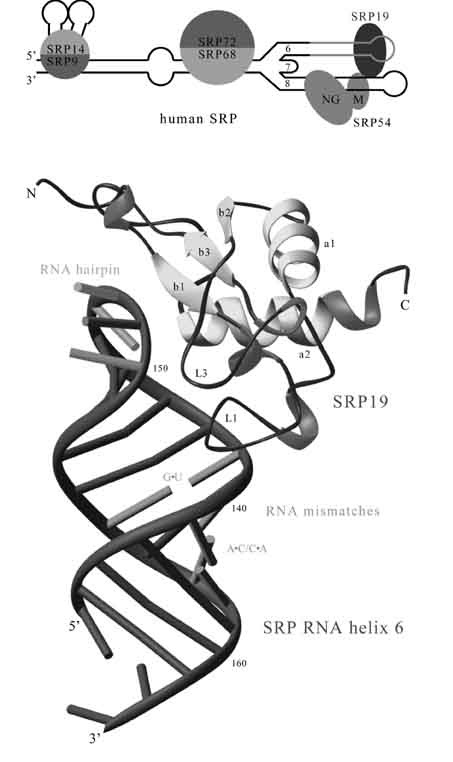
Wichtig für das Verständnis der Funktionsweise der Proteinzielsteuerung ist die Kenntnis der atomaren Strukturen des SRP, die durch die Methode der Röntgenstrukturanalyse erhalten werden kann. In einem solchen Experiment beschreiben die Autoren die Struktur eines wichtigen Protein-RNA-Teilkomplexes, verantwortlich für die innere Organisation des humanen SRP. Die hohe Auflösung von 0.18 nm der Struktur (Protein SRP19 mit 29 Nukleotiden der SRP RNA helix 6) erlaubt atomare Aussagen über den Aufbau der Bestandteile sowie der Protein-RNA-Interaktionen.
So konnten neue Faltungsmuster, wie die einer speziellen RNA-Haarnadelschleife, identifiziert werden und auch die Wichtigkeit von strukturierten Wassermolekülen als molekularem Fugenkitt in Protein-RNA-Komplexen demonstriert werden. Anhand der gewonnenen Daten lässt sich nun wie in einem Baukastensystem zusammen mit anderen, bereits bekannten Kristallstrukturen ein Teilmodell des SRP erstellen und die komplexe Organisation des Partikels besser verstehen. Die Autoren sind zuversichtlich, dieses Modell des zellulären Briefträgers SRP in einem durch das europäische "framework V" geförderten Forschungsvorhaben bald durch eine komplexere Kristallstruktur mit zusätzlichen SRP-Komponenten ersetzen zu können.
Rückfragen bitte an:
Prof. Dr. Irmgard Sinning
Universität Heidelberg
Biochemie-Zentrum Heidelberg (BZH)
Tel. 06221 544781, Fax 544790
irmi.sinning@bzh.uni-heidelberg.de
allgemeine Rückfragen von Journalisten auch an:
Dr. Michael Schwarz
Pressesprecher der Universität Heidelberg
Tel. 06221 542310, Fax 542317
michael.schwarz@rektorat.uni-heidelberg.de
Die semantisch ähnlichsten Pressemitteilungen im idw