Preisgekrönte Forschungsrichtung auch an Universität Bayreuth prominent vertreten
Am Donnerstag Richtfest für NMR-Halle - Spektrometer der höchsten Leistungsklasse. Das Kernstück eines solchen Spektrometers ist ein etwa 4 m hoher, mit flüssigem Helium gekühlter Magnet.
Bayreuth (UBT). Die vergangene Woche bekannt gegebenen Chemie-Nobelpreise gingen an drei Wissenschaftler, bemerkenswerterweise nur einer von ihnen ausgebildeter Chemiker, die zwei verschiedene Methoden zur Analyse von biologischen Makromolekülen, zum Beispiel Proteinen, (weiter-)entwickelten und erfolgreich einsetzten. Mit diesen Arbeitsgebieten beschäftigen sich auch Bayreuther Wissenschaftler intensiv und können bald auf verbesserte Bedingungen hoffen.
Diese Methoden, Biomoleküle im Detail zu analysieren und ihre Gestalt zu bestimmen, haben das Verständnis der Lebensprozesse grundsätzlich erweitert. Beide Methoden haben vor allem die Entwicklung neuer Medikamente revolutioniert. Neue und viel versprechende Anwendungen werden laufend auch aus anderen Bereichen gemeldet.
Die beiden Methoden, Massenspektrometrie und magnetische Kernresonanz (nuclear magnetic resonance, NMR), werden in ihrer grundlegenden Form in praktisch jedem Chemielaboratorium angewendet. Aber auch außerhalb der Chemie sind Massenspektrometrie und NMR von überragender Bedeutung, etwa in der Lebensmittelkontrolle, der Routine-Medizin (Kernspintomographen) oder der kriminalistischen Analytik. Die Massenspektrometrie ist vergleichbar einer hoch empfindlichen Balkenwaage, mit der die Massen ("Gewichte") von Molekülen äußerst genau bestimmt werden können. Die NMR nutzt die magnetischen Eigenschaften von Atomkernen aus, ihre Anwendung zielt auf die Bestimmung der räumlichen Strukturen und der Bewegungen von Molekülen.
Mit Massenspektrometrie konnten ursprünglich nur sehr kleine Moleküle "gewogen" werden, aber die diesjährigen Chemienobelpreisträger John B. Fenn und Koichi Tanaka haben Methoden entwickelt, die auch die Analyse großer biologischer Moleküle ermöglichen. Fenn ist seit 1987 im Ruhestand und veröffentlichte 1988 seine entscheidende Arbeit über die so genannte "electrospray ionization" Methode, was ihm nun den Nobelpreis einbrachte. Mit "electrospray ionization" werden zuerst geladene Tröpfchen einer Lösung von Protein in Wasser produziert, die dann wegen des im Vakuum verdunstenden Wasseranteils zusammenschrumpfen. Die übrig bleibenden Proteinionen schweben, werden beschleunigt und ihre Flugzeit über eine bekannte Strecke wird gemessen. Hieraus kann man die Masse der Proteine berechnen.
Gleichzeitig führte Koichi Tanaka eine andere Technik ein, um im Vakuum schwebende Proteinionen zu erzeugen, nämlich die "weiche Laserdesorption". Ein Laserpuls wird auf die Probe gerichtet, die in kleine Teile "gesprengt" wird und somit die Moleküle frei gibt. Fenn und Tanaka erhielten je ein Viertel des diesjährigen Preises (gesamter Preis: ca. 1.1 Mio. Euro).
Während die Massenspektrometrie im Wesentlichen die Bestimmung der Masse von Biomolekülen erlaubt, gestattet die NMR die Form dieser Moleküle im Detail zu untersuchen. Es gibt zurzeit zwei Methoden, mit denen man die räumliche Gestalt von Biomolekülen aufklären kann, die Röntgenkristallographie und die NMR. Der Vorteil der NMR liegt darin, dass man die Proteine in Lösung, also in einer den Verhältnissen in lebenden Zellen sehr ähnlichen Umgebung studieren kann. Die Hälfte des Nobelpreises ging an den Schweizer Biophysiker Kurt Wüthrich, Direktor des Instituts für Biophysik an der Eidgenössischen Technischen Hochschule (ETH) Zürich, für die Weiterentwicklung dieser Methode und ihren Einsatz zur Aufklärung der räumlichen Struktur von Proteinen.
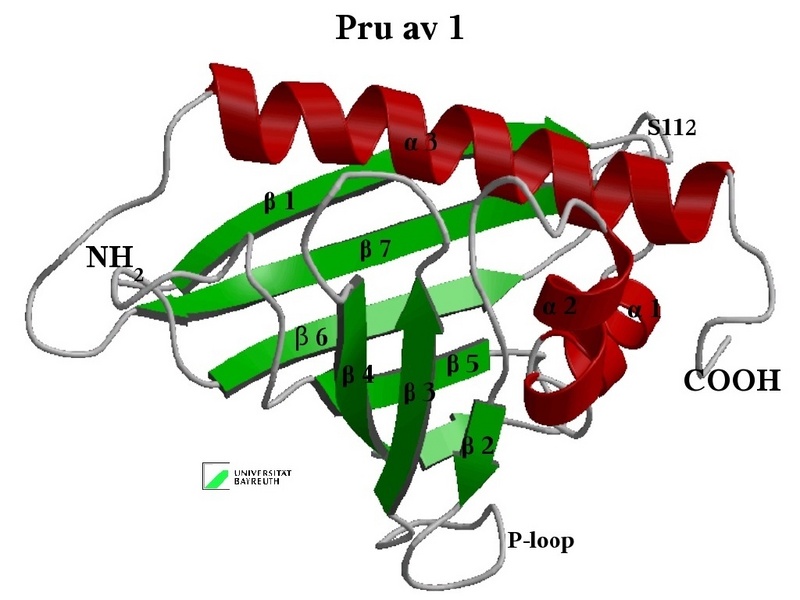
Auch an der Universität Bayreuth ist dieser Zweig der biophysikalischen Forschung ein Schwerpunkt: Die hier durchgeführten Arbeiten unter Verwendung der NMR-Spektroskopie an biologischen Makromolekülen konzentrieren sich auf medizinisch relevante Forschung beispielsweise auf den Gebieten HIV, BSE und Allergien. Die typische räumliche Struktur eines Proteins, das Allergien wie etwa Heuschnupfen verursacht, wurde in Bayreuth aufgeklärt.
Die Bestimmung einer solchen Struktur ist noch immer keine Routinearbeit, sondern erfordert einen hohen zeitlichen und finanziellen Einsatz. Diese Strukturen können dann aber als Grundlage für die Konstruktion neuer Arzneimittel verwendet werden.
In den nächsten Monaten wird die Universität Bayreuth die Ausstattung der Arbeitsrichtung erheblich verbessern und sich damit auf diesem Gebiet weltweit mit an die Spitze stellen. Eine neue Gerätehalle mit 500 m² Grundfläche und über 8 m Höhe geht derzeit ihrer Vollendung entgegen- am kommenden Donnerstag (17. Oktober) ist Richtfest.
Bestückt wird die Halle in Kürze mit zwei Spektrometern der höchsten derzeit erhältlichen Leistungsklasse. Das Kernstück eines solchen Spektrometers ist ein etwa 4 m hoher, mit flüssigem Helium gekühlter Magnet, in den die zu untersuchende Probe mit einem Volumen von nur etwa 0.4 cm3 gebracht wird. Ergänzt wird dieser Forschungsbereich durch eine neu eingerichtete Professur für Bioinformatik. Dass sich diese Investition lohnt, zeigt sich unter anderem daran, dass der mit diesem Gebiet befasste Lehrstuhl Biopolymere (Leiter: Professor Dr. Paul Rösch) gerade in der letzten Woche für seine Beiträge zur HIV- und BSE-Forschung wieder die Genehmigung erheblicher Mittel des Bayerischen BSE-Forschungsverbundes und der Deutschen Forschungsgemeinschaft mitgeteilt bekam.
Die semantisch ähnlichsten Pressemitteilungen im idw